¿Qué pueden tener en común 1.300.000 especies que
difieren tanto entre sí como los hombres y las lombrices de tierra, las
ballenas y las ostras, las alondras y el musgo, los robles y los renacuajos,
las algas marinas y los elefantes? (Y esto sin mencionar los muchos millares, o
incluso millones, de especies extintas desde los trilobites hasta la boa
gigante.)
El ojo humano solo no puede dar la respuesta. Sin
embargo, mediante el uso del microscopio, se obtuvo la respuesta hace mucho
tiempo. En 1838, un botánico alemán, Matthias J. Schleiden, sugirió que todas
las plantas estaban formadas por unidades microscópicas separadas llamadas
células. En 1839, un zoólogo alemán, Theodor Schwann, extendió esta noción a
los animales.
Cada célula es una unidad independiente, separada
de las demás por una membrana y capaz de demostrar en sí misma las diversas
habilidades asociadas con la vida. Una célula, o partes de ella, puede moverse,
sentir y responder, transformarse por metabolismo, crecer y reproducirse.
Los organismos lo bastante grandes como para ser
vistos sin ayuda de instrumentos están formados por un número mayor de células.
Un ser humano adulto contiene unos cincuenta billones (50.000.000.000.000).
Cada célula en un organismo multicelular semejante está tan adaptada a la
presencia de las demás que ya no puede vivir aislada. Sin embargo, hay algunas
células que, en realidad, son capaces de vivir independientemente. La mayor
parte de las formas de criaturas microscópicas están formadas de células
únicas; son organismos unicelulares. E incluso las criaturas mayores empiezan
su vida como células únicas. Cada ser humano tiene su comienzo como un óvulo
fecundado: una célula.
No obstante, aunque los organismos pueden variar
enormemente, las células microscópicas de que están compuestos no se
diferencian apenas. Una célula de ballena se parece mucho más a una célula de
ratón que la ballena en sí se parece al ratón.
Todas las plantas y animales están formados de
células, y las partes de un organismo vivo que no están compuestas de células
activas no están vivas. (La corteza de un árbol no está viva, ni el pelo de un
animal, ni las plumas de un ave, ni las conchas de una ostra; lo cual no quiere
decir que el organismo pueda vivir necesariamente sin esa porción no viviente.)
Ninguna cosa no viva está formada de células activas; aunque un organismo
recién muerto está formado por células muertas. (Algunas células pueden seguir
viviendo brevemente después de la muerte de la criatura; sin embargo, antes de
que pase mucho tiempo, todas las células mueren)
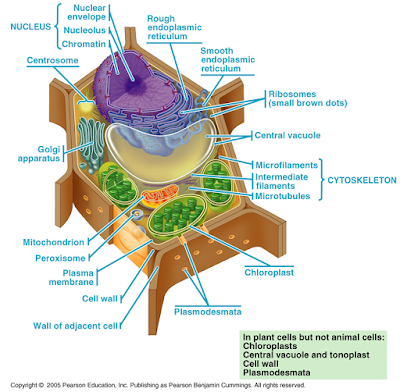 |
Célula vegetal |
 |
Célula animal |
Las células contienen una mezcla enormemente
compleja de sustancias, pero éstas están formadas sólo por unos pocos
elementos. Casi todos los átomos que contienen son de unas seis clases
diferentes: carbono, oxígeno, hidrógeno, nitrógeno, fósforo y azufre. Hay
cantidades menores de otros átomos, tales como de hierro, calcio, magnesio,
sodio, potasio, e indicios de cobre, cobalto, cinc, manganeso y molibdeno. Sin
embargo, no hay nada en estos elementos en sí que dé ninguna clave acerca de la
naturaleza de la vida. También son bastante comunes en las cosas no vivas.
Los átomos en la célula están agrupados en
moléculas que, en líneas generales, se clasifican en tres tipos: glúcidos, lípidos y proteínas.
 |
La sacarosa, el azúcar que comemos, es un ejemplo de glúcido |
De éstos, las moléculas de la proteína son, con
mucho, las más complejas. Mientras que las moléculas de hidratos de carbono y
lípidos suelen estar formadas por átomos de carbono, hidrógeno y oxígeno
solamente, las proteínas invariablemente incluyen también átomos de nitrógeno y
de azufre. Mientras que las moléculas de hidratos de carbono y de lípidos
pueden ser descompuestas en simples unidades de dos a cuatro clases, la
molécula proteínica puede ser descompuesta en unidades simples (aminoácidos) de
no menos de veinte variedades diferentes.
 |
Aminoácidos |
Las proteínas son de particular importancia en
relación con los millares de diferentes reacciones químicas que se producen
constantemente en las células. La velocidad de cada reacción diferente es
controlada por una clase de moléculas proteínicas llamadas enzimas: una enzima
diferente para cada reacción. La célula contiene un gran número de enzimas
diferentes, cada una presente en ciertas cantidades y, a menudo, en ciertas
posiciones dentro de la célula. El modelo de la enzima determina el modelo de
las reacciones químicas y, de este modo, controla la naturaleza de la célula y
las características del organismo constituido a base de las células.
Las propiedades de la molécula de las enzimas
depende de la particular disposición de aminoácidos que posea. El número de
disposiciones posibles es inconcebiblemente grande. Si una molécula está
formada por 500 aminoácidos de 20 clases diferentes (el promedio de una
proteína), el número total de disposiciones posibles puede llegar a ser hasta
de 101100 (una cifra que podemos escribir como un 1 seguido por 1.100 ceros).
Entonces, ¿cómo consigue la célula formar la particular disposición necesaria
para obtener enzimas particulares de todas esas posibilidades?
La respuesta a esta pregunta parece hallarse en
los cromosomas, pequeñas estructuras filiformes en un pequeño cuerpo llamado el
núcleo, habitualmente situado cerca del punto central de la célula. Cuando la
célula está en proceso de división, cada cromosoma forma otro justamente igual
que él mismo (réplica). Las dos células hijas formadas al final de la división
tienen su propio juego duplicado de cromosomas.
 |
Mitosis o división celular |
Los cromosomas están formados de proteína
asociada con una célula aún más compleja llamada ácido desoxirribonucleico,
usualmente abreviado como ADN. El ADN contiene en su propia estructura la
«información» necesaria para la construcción de enzimas específicas, así como
para la reproducción de sí misma a fin de poder continuar la construcción de
enzimas específicas en las células hijas. Cada criatura posee las moléculas ADN
para formar sus propias enzimas, y no otra.
 |
| Cariotipo humano ( conjunto de cromosomas de una célula humana, con la información para todo el organismo) |
 |
| Del cromosoma al ADN |
¿Es posible que igual que ciertos organismos
pueden consistir en células individuales, otros aún más simples puedan
consistir en cromosomas individuales? Aparentemente, así es, pues los virus son
muy semejantes a cromosomas individuales e independientes.
Cada virus está compuesto de una capa exterior de
proteína y una molécula interior de ADN (o, en algunos casos, una molécula
similar, ácido ribonucleico o ARN). El ADN o ARN consigue introducirse en una
célula y allí supervisa la producción de enzimas designadas para producir más
moléculas víricas del tipo exacto que invadió la célula. El problema es que solo puede reproducirse parasitando a otra célula.
Las criaturas vivas representan diferentes
niveles de complejidad y organización. Una criatura grande suele ser más
compleja que una pequeña del mismo tipo, al menos porque tiene más partes
interrelacionadas. Por lo general, los animales son más complejos que las plantas.
Por ejemplo, los animales tienen tejidos particularmente complejos, tales como
los músculos y los nervios, de los que carecen las plantas. A causa de esto, se
puede considerar que un ratón es más complejo que un roble.
Las estructuras más complejas que se hallan en el
organismo animal son los cerebros; y éstos son sumamente complejos en ciertos
mamíferos. El que posee mayor cerebro es el hombre, junto con los elefantes y
las ballenas. Por ejemplo, el cerebro humano pesa alrededor de un kilo y
trescientos sesenta gramos y está compuesto por diez mil millones de células
nerviosas conectadas quizás a otras mil, siendo cada célula nerviosa individual
enormemente compleja por sí misma. Estudiando más la complejidad de los
cerebros de elefantes y ballenas, parece oportuno decir que el cerebro humano
es la cosa más altamente organizada que conocemos.
Naturalmente, este nivel de organización no se
consiguió de sopetón, sino que fue el producto de, como mínimo, tres mil
millones de años de lentos cambios. Los propios cambios se produjeron por
casuales imperfecciones en las réplicas de ADN, lo cual condujo a los
correspondientes cambios en la estructura de la enzima y, con ello, del modelo
de reacción en las células. Estos cambios particulares sobrevivieron porque, por
una u otra razón, resultaron beneficiosos para el organismo en las particulares
condiciones que lo rodeaban. (Tal teoría de la evolución por la selección
natural fue publicada la primera vez por el biólogo inglés Charles Darwin, en
1859.)
Fragmento adaptado de un texto de Isaac Asimov , del libro Tiempo y vida
Referente a este texto, escribe:
1- Dos conceptos que te hayan sorprendido, que te hayan llamado la atención.
2- Dos conceptos que no conocías y de los que te gustaría conocer más.
3- Dos conceptos que no hayas comprendido.
Referente a este texto, escribe:
1- Dos conceptos que te hayan sorprendido, que te hayan llamado la atención.
2- Dos conceptos que no conocías y de los que te gustaría conocer más.
3- Dos conceptos que no hayas comprendido.











